Luftvägsremodellering vid astma: Varför det är viktigt att rikta in sig på IL-4 och IL-131,9
Luftvägsremodellering driver en progressiv och potentiellt irreversibel försämring av lungfunktionen vid astma.2 Att förstå IL-4:s och IL-13:s centrala roll i denna process är avgörande för effektiva behandlingsstrategier.1,10
Lyssna på professor Alberto Papi prata om luftvägsremodellering
Förstå luftvägsremodellering och hyperreaktivitet1,3-5
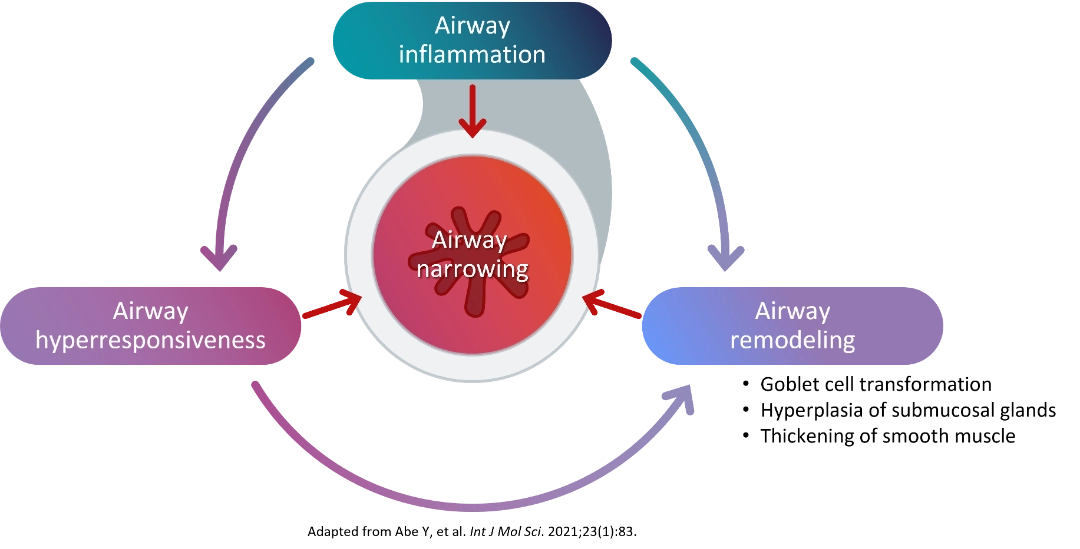
Astma innebär kronisk luftvägsinflammation, strukturella förändringar i luftvägarnas epitel och en överdriven luftvägsförträngning vid stimuli.3,4 Dessa processer – luftvägsremodellering och luftvägshyperreaktivitet (AHR) – är nyckelmekanismer bakom försämrad lungfunktion och sjukdomsprogression.1,5
Typ 2 inflammation, hyperreaktivitet och remodellering bidrar till luftvägsförträngning6 |
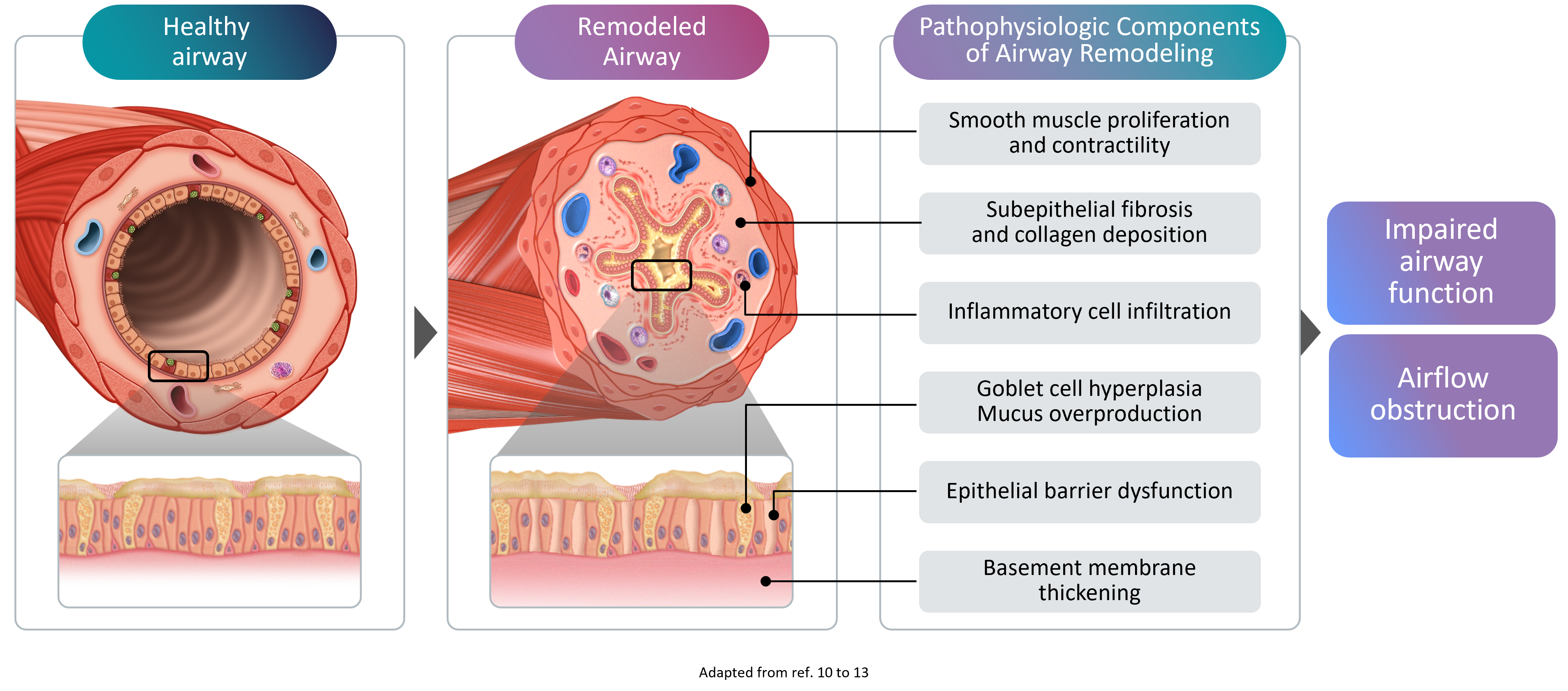
Luftvägsremodellering avser de progressiva strukturella förändringar i luftvägarna som uppstår till följd av kronisk inflammation. Dessa inkluderar:
- Förtjockning av det retikulära basalmembranet — lagret under luftvägsepitel blir onormalt tjockt
- Subepitelial fibros — överskott av ärrvävnad under ytan
- Hypertrofi av glatt muskulatur (ASM) — muskelcellerna som omger luftvägarna ökar i storlek
- Gobletcellshyperplasi — ökad mängd slemproducerande celler leder till överdriven slemproduktion4
Luftvägsremodellering i astma omfattar strukturella förändringar i luftvägarna10-13
AHR är luftvägarnas överdrivna tendens att dra ihop sig som svar på stimuli.
Mekanismer:
- Ökad kontraktilitet i glatt muskulatur
- Ihållande luftvägsinflammation
- Strukturella förändringar från remodellering3,5
Nyckelinsikt |
AHR är kopplat till ökad risk för lungfunktionsförsämring, kvarstående symtom och framtida exacerbationer. Behandlingsstrategier som normaliserar AHR kan minska risken för exacerbationer och hindra fortsatt inflammation och remodellering.5 |
Typ 2 inflammationens roll10
Majoriteten av patienter med astma har typ 2 inflammation som drivande patofysiologisk mekanism.10
Drivs av cytokinerna:
- IL-4
- IL-13
- IL-5
- Alarminer (ex. TSLP)
Hur typ 2 cytokiner driver astmapatologi?1-2,10-11
Kombinerad effekt: Ödem, slemhypersekretion, AHR, remodellering → sänkt lungfunktion.10
Visste du? |
Eosinofiler är inte den huvusakliga drivkraften av luftvägsremodellering. IL-4 och IL-13 är de cytokiner som huvudsakligen orsakar de strukturella förändringar som leder till lungfunktionsförsämring.1,2 |
Typ 2 cytokiners roll vid remodellering
IL-4 |
IL-13 |
IL-5 |
| T- och B-cellsdifferentiering | ||
|
|
Eosinofildifferentiering i benmärgen | |
| Migration och extravasation av eosinofiler in i lungans luftvägar | ||
| IgE produktion och klassbyte; degranulering av mastceller och basofiler |
||
| Gobletcellsmognad; slemsekretion |
||
| Differentiering av bronkialepitelceller | ||
| Ökad kontraktilitet i luftvägarnas glatta muskelceller och bronkiell hyperreaktivitet | ||
Observera: Det tymiska stromala lymfopoietinet (TSLP), en epitelhärledd cytokin, bidrar till luftvägsremodellering i lungorna genom att underlätta differentieringen av T hjälparceller typ 2 (Th2) och påverka dendritcellernas funktion.
IL-4 och IL-13: Kritiska terapeutiska mål1,8,9
Även om eosinofiler och IL-5 är viktiga markörer för exacerbationer är IL-4 och IL-13 de primära drivkrafterna bakom strukturella förändringar.2 Att rikta behandling mot IL-4 och IL-13 adresserar både inflammationen och remodelleringen.2
Även om eosinofilantal och IL-5 är viktiga markörer för astmaexacerbationer, är IL-4 och IL-13 de primära drivkrafterna bakom de strukturella luftvägsförändringar som ses vid remodellering. Terapeutiska behandlingsstrategier som riktar sig mot IL-4 och IL-13 kan påverka både den inflammatoriska kaskaden och de underliggande remodelleringsprocesser som bidrar till försämrad lungfunktion.1,8,9
Jämförelse av terapeutiska mål
Mål |
Mekanism |
Effekt på remodellering |
| IL-4 & IL-131,2,9 | Driver inflammation, eosinofilmigration, slemsekretion, AHR. | Direkt minskning av remodellering. |
| IL-51,2 | Påverkar eosinofiler. | Indirekt effekt via minskad eosinofil aktivitet. |
Viktig notering |
Blockad av IL-4 och IL-13 kan:minska eosinofilinfiltration, dämpa typ 2 inflammation, ge behandlingseffekter som går utöver eosinofilreduktion1,2 |
Kliniska implikationer: Vikten av tidig intervention7
Luftvägsremodellering är progressiv och tidigt ingripande som riktar sig mot inflammationsdrivarna kan:
- minska akuta attacker
- förhindra irreversibel lungfunktionsförlust
Biomarkörer att bedömma:
- Blodeosinofiler
- FeNO
- Serum IgE
Klinisk rekomendetaion |
Identifiera patienter i risk för remodellering genom tidig biomarkörsbedömning. Proaktiv fenotypning och riktad intervention kan förbättra sjukdomsprognosen.7 |
Lyssna till professor Alberto Papi prata om vikten av tidig intervention
-
Nakagome K, Nagata M. The Possible Roles of IL-4/IL-13 in the Development of Eosinophil-Predominant Severe Asthma. Biomolecules. 2024;14(5):546. Published 2024 May 2. doi:10.3390/biom14050546
-
Scott G, Asrat S, Allinne J, et al. IL-4 and IL-13, not eosinophils, drive type 2 airway inflammation, remodeling and lung function decline. Cytokine. 2023;162:156091. doi:10.1016/j.cyto.2022.156091
-
Bradding P, Porsbjerg C, Côté A, Dahlén SE, Hallstrand TS, Brightling CE. Airway hyperresponsiveness in asthma: The role of the epithelium. J Allergy Clin Immunol. 2024;153(5):1181-1193. doi:10.1016/j.jaci.2024.02.011
-
Hough KP, Curtiss ML, Blain TJ, et al. Airway Remodeling in Asthma. Front Med (Lausanne). 2020;7:191. Published 2020 May 21. doi:10.3389/fmed.2020.00191
-
Chapman DG, Irvin CG. Mechanisms of airway hyper-responsiveness in asthma: the past, present and yet to come. Clin Exp Allergy. 2015;45(4):706-719. doi:10.1111/cea.12506
-
Abe Y, Suga Y, Fukushima K, et al. Advances and Challenges of Antibody Therapeutics for Severe Bronchial Asthma. Int J Mol Sci. 2021;23(1):83. Published 2021 Dec 22. doi:10.3390/ijms23010083
-
Zhang J, Dong L. Status and prospects: personalized treatment and biomarker for airway remodeling in asthma. J Thorac Dis. 2020;12(10):6090-6101. doi:10.21037/jtd-20-1024
-
León B, Ballesteros-Tato A. Modulating Th2 Cell Immunity for the Treatment of Asthma. Front Immunol. 2021;12:637948. Published 2021 Feb 10. doi:10.3389/fimmu.2021.637948
-
Pelaia C, Heffler E, Crimi C, et al. Interleukins 4 and 13 in Asthma: Key Pathophysiologic Cytokines and Druggable Molecular Targets. Front Pharmacol. 2022;13:851940. Published 2022 Mar 8. doi:10.3389/fphar.2022.851940
-
Gandhi NA, et al. Nat Rev Drug Discov. 2016;15(1):35-50.
-
Israel E, Reddel HK. N Engl J Med. 2017;377(3):965-976.
-
Mauad T, et al. J Allergy Clin Immunol. 2007;120(5):997-1009.
-
Robinson D, et al. Clin Exp Allergy. 2017;47(2):161-175.