- Artículo
- Fuente: Campus Sanofi
- 15 mar 2021
La inflamación crónica en dermatitis atópica
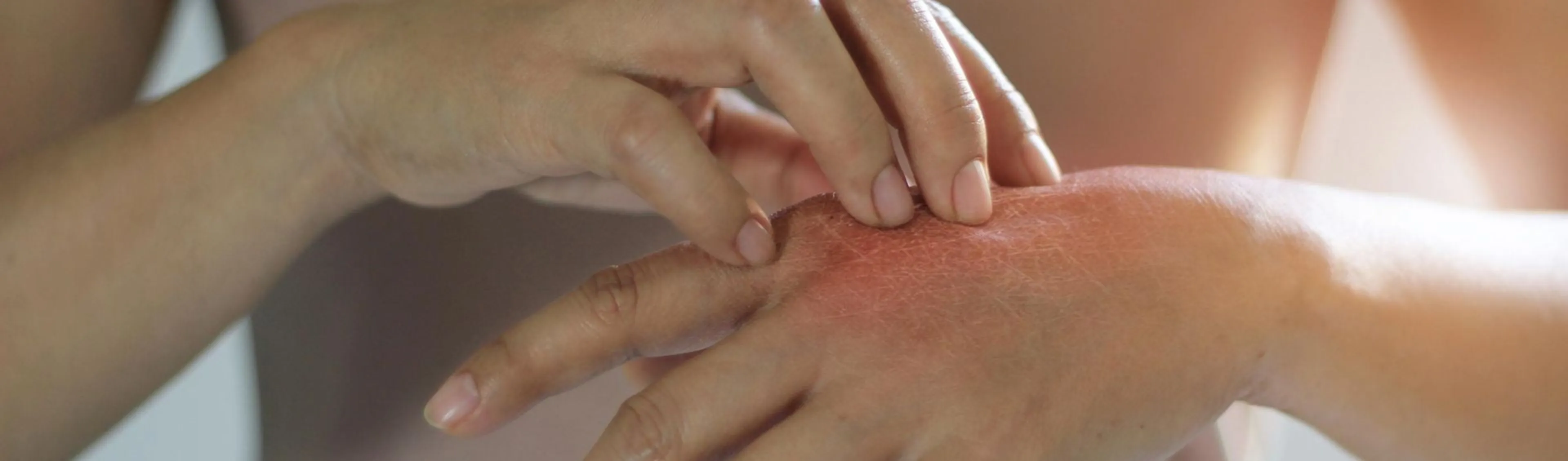
Los datos actuales demuestran que la piel sin lesiones no es piel sana.1-4 La inflamación crónica de la piel puede deberse a la infiltración de células inmunitarias y epidérmicas, que generan lesiones
pruriginosas.5-11 Cada vez es más generalizada la teoría de que la epidermis de la piel con dermatitis atópica es hipersensible a los factores medioambientales, y que presenta una hiperactividad celular subyacente en las capas profundas de la piel.
- La piel sin lesiones y aparentemente sana de estos pacientes presenta un aumento de la sequedad y una mayor respuesta a los irritantes frente a los controles sanos2
Experimentos en modelos murinos y cultivos celulares de piel humana dejan entrever que la inflamación originada por Th2 debilita la barrera cutánea y causa xerosis (es decir, sequedad anómala de la piel) así como lesiones extremadamente pruriginosas.12,13
- La xerosis, las infecciones y los alérgenos contribuyen al prurito, que puede14,15:
- Iniciar el ciclo picor-rascado.
- Dañar la barrera cutánea.
- Exacerbar los signos y los síntomas.
- Los estudios en animales han demostrado que el daño a la capa córnea provoca la liberación de neuromediadores por parte de los queratinocitos y el aumento de fibras nerviosas en la epidermis, lo que incrementa el prurito.15
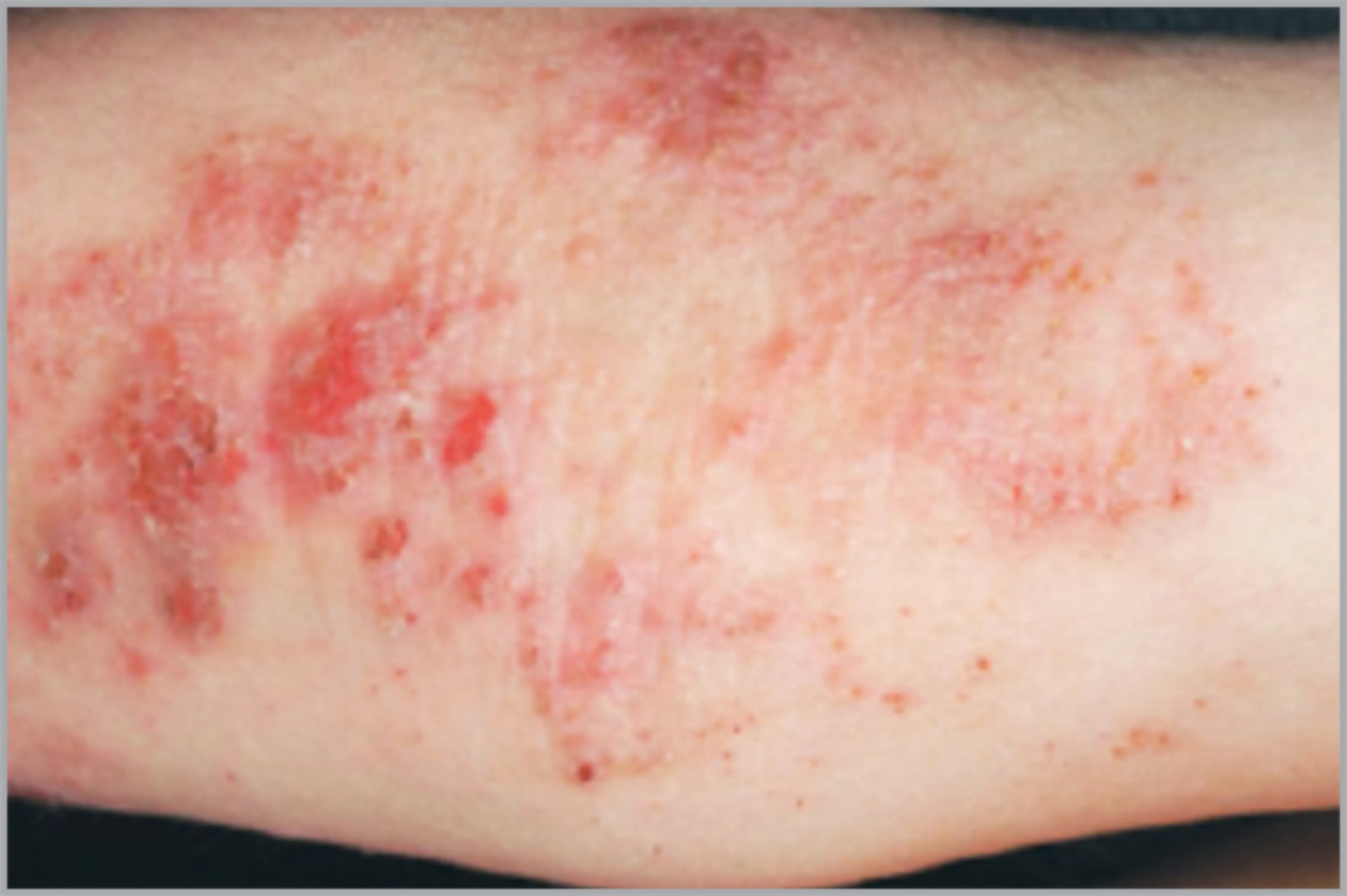
Publicado en J Derm Sci, Bieber T, Mechanisms of disease: atopic dermatitis. 2008;358(14):1483-1494. © 2016 Massachusetts Medical Society. Reimpresa con permiso de Massachusetts Medical Society.16
La dermatitis atópica es una enfermedad inflamatoria crónica en la que las citocinas de tipo Th2 IL-4 e IL-13 son factores clave implicados en el proceso inflamatorio subyacente.1
Temas relacionados
#Inflamación tipo 2
Referencias
- Gittler JK, Shemer A, Suárez-Fariñas M, et al. Progressive activation of TH2/TH22 cytokines and selective epidermal proteins characterizes acute and chronic atopic dermatitis. J Allergy Clin Immunol. 2012;130(6):1344-1354.
- Leung DYM, Boguniewicz M, Howell MD, Nomura I, Hamid QA. New insights into atopic dermatitis. J Clin Invest. 2004;113(5):651-657.
- Suárez-Fariñas M, Tintle SJ, Shemer A, et al. Nonlesional atopic dermatitis skin is characterized by broad terminal differentiation defects and variable immune abnormalities. J Allergy Clin Immunol. 2011;127(4):954-964.
- De Benedetto A, Rafaels NM, McGirt LY, et al. Tight junction defects in patients with atopic dermatitis. J Allergy Clin Immunol. 2011;127(3):773-786.
- Gaffal E, Glodde N, Jakobs M, Bald T, Tüting T. Cannabinoid 1 receptors in keratinocytes attenuate fluorescein isothiocyanate-induced mouse atopic-like dermatitis. Exp Dermatol. 2014;23(6):401-406.
- Kagami S, Kakinuma T, Saeki H, et al. Significant elevation of serum levels of eotaxin-3/CCL26, but not of eotaxin-2/CCL24, in patients with atopic dermatitis: serum eotaxin-3/CCL26 levels reflect the disease activity of atopic dermatitis. Clin Exp Immunol. 2003;134(2):309-313.
- Owczarek W, Paplińska M, Targowski T, et al. Analysis of exotoxin 1/CCL11, exotoxin 2/CCL24 and exotoxin 3/CCL26expression in lesional and non-lesional skin of patients with atopic dermatitis. Cytokine. 2010;50(2):181-185.
- Akdis M, Akdis CA, Weigl L, Disch R, Blaser K. Skin-homing, CLA+ memory T cells are activated in atopic dermatitis and regulate IgE by an IL-13-dominated cytokine pattern: IgG4 counter-regulation by CLA-memory T cells. J Immunol. 1997;159(9):4611-4619.
- Akdis M, Simon H-U, Weigl L, Kreyden O, Blaser K, Akdis CA. Skin homing (cutaneous lymphocyte-associated antigen-positive) CD8+ T cells respond to superantigen and contribute to eosinophilia and IgE production in atopic dermatitis. J Immunol. 1999;163(1):466-475.
- Seneviratne SL, Black AP, Jones L, Bailey AS, Ogg GS. The role of skin-homing T cells in extrinsic atopic dermatitis. Q J Med.2007;100(1):19-27.
- Jung T, Moessner R, Neumann C. Naïve CD4+ T cells from patients with atopic dermatitis show an aberrant maturation towards IL-4 producing skin-homing CLA+ cells. Exp Dermatol. 2003;12(5):555-562.
- Hatano Y Adachi Y, Elias PM, et al. The Th2 cytokine, interleukin-4, abrogates the cohesion of normal stratum corneum in mice: implications for pathogenesis of atopic dermatitis. Exp Dermatol. 2013;22(1):30-35.
- Kabashima K. New concept of the pathogenesis of atopic dermatitis: interplay among the barrier, allergy, and pruritus as a trinity. J Derm Sci. 2013;70(1):3-11.
- Brandt EB, Sivaprasad U. Th2 cytokines and atopic dermatitis. J Clin Cell Immunol. 2011;2(3). doi:10.4172/2155-9899.1000110.
- Yosipovitch G, Papoiu ADP. What causes itch in atopic dermatitis? Curr Allergy Asthma Reports. 2008;8(4):306-311.
- Bieber T. Mechanisms of disease: atopic dermatitis. N Engl J Med. 2008;358(14):1483-1494.

Realice el Test de Control de dermatitis atópica (ADCT)
La dermatitis atópica, un tipo de eccema, puede estar afectando la vida de su paciente en más formas de las que cree.
El ADCT da una medida de qué tan controlado está el eczema. Responda estas 6 preguntas simples con su paciente para encontrar la puntuación ADCT. Indicará el curso de acción adecuado.
Encuentre la puntuación de su paciente