- Artículo
- Fuente: Campus Sanofi
- 1 jun 2021
Eczema de contacto irritativo
Introducción
La piel es la principal barrera de nuestro cuerpo frente a los agentes físicos, químicos y biológicos. Afortunadamente, la mayoría de estas exposiciones no produce alteraciones clínicamente visibles, sin embargo, en algunas circunstancias, esta exposición produce una serie de acontecimientos patogénicos que van a desencadenar una cascada inflamatoria que puede provocar lesiones clínicas en forma de eczema. Los eczemas son patrones de reacción cutánea definidos por sus características clínicas (eritema, pápulas, vesículas, liquenificación), cuyo sustrato histológico fundamental es la espongiosis epidérmica y que pueden tener un origen muy variado. En ocasiones pueden estar provocados por factores endógenos, como en el eczema atópico, mientras que en otras se producen por factores externos, denominándose en estos casos eczema de contacto. El eczema de contacto supone la mayoría de los casos de enfermedades profesionales cutáneas1, tiende a ser crónico y conlleva una carga económica importante, llevando en muchos casos a perder el trabajo, además de producir una disminución de la calidad de vida. Este tipo de eczema se puede dividir en eczema alérgico de contacto (EAC), fundamentado por una reacción de hipersensibilidad tipo IV ante antígenos que entran en contacto con la piel, y eczema de contacto irritativo (ECI), que se produce por una reacción inflamatoria no específica en respuesta a una exposición única o repetida a una sustancia irritante.
Los objetivos principales de este capítulo son los siguientes:
-
Definir los fenómenos fisiopatológicos que se producen y los principales factores condicionantes del ECI.
-
Repasar las diferentes formas clínicas del ECI, su prevención y tratamiento
Contenido relacionado
Epidemiología
Clásicamente se ha considerado que los ECI representan un 80% de las enfermedades profesionales cutáneas (EPC)2 y que el resto eran fundamentalmente EAC. Sin embargo, en una revisión publicada en 19943 ya se constató que había importantes diferencias en los estudios publicados sobre EPC, entre los porcentajes de EAC y ECI. En los estudios más recientes los porcentajes varían dependiendo de las zonas geográficas y de las ocupaciones. Por ejemplo en Australia desde 1993 a 2014 el porcentaje de ECI en sanitarios con EPC era del 79,1%4. En EE.UU. en un estudio del North American Contact Dermatitis Research Group (NACDRG) sobre EPC en los pacientes que acudían a realizar pruebas epicutáneas desde 1998 a 20005 se comunicaron muchos más casos de ECA (60%) que de ECI (32%). Otro estudio del European Surveillance System on Contact Allergies (ESSCA) realizado desde 2002 a 2010 entre pacientes que acudieron a realizar pruebas epicutáneas por sospecha de EPC, el porcentaje de ECI fue del 28,7%6 y el de EAC fue del 35,3%, aunque en su estudio había un 10,7% de pacientes que tenían un EAC y un ECI de forma concomitante, algo que no se ha reflejado en otros estudios y que en la práctica clínica se ve de forma frecuente7.
Esas diferencias en la prevalencia del ECI pueden ser debidas a múltiples factores8: al tipo de industria presente en una determinada zona geográfica, a diferencias en el sexo y edad de los pacientes estudiados, a la metodología seguida por los médicos que recogen los datos y a diferencias en los sistemas de notificación o en las regulaciones nacionales, sin embargo, es probable que la mayoría de estos registros tengan sesgos de selección, ya que los eczemas de contacto irritativo son más leves y muchos de esos pacientes no son referidos a centros terciarios para estudio. Por último también es posible que muchos estudios tengan sesgos de información, ya que para diferenciar de forma adecuada entre un EAC y un ECI es imprescindible realizar pruebas epicutáneas, cuya ejecución e interpretación está sometida a una notable variabilidad interoperador9
Fisiopatología
La dermatitis irritativa se considera como una interacción compleja de eventos que incluye la degradación de la barrera cutánea, cambios celulares y la liberación de numerosos mediadores proinflamatorios y antiinflamatorios. Los irritantes inducen una respuesta inmunitaria fundamentalmente innata10. Esta respuesta es mediada inicialmente a través de los receptores de tipo toll (TLR), presentes en la membrana celular, y los receptores tipo NOD (NLR), que detectan esas señales de peligro y activan las vías de señalización inflamatoria11.
Las sustancias irritantes pueden producir ligandos para los TLR, activar el inflamosoma y la vía NFκB. Esta activación de la inmunidad innata desencadena una activación de múltiples vías de señalización intracelular como las proteínas adaptadoras de transducción de señal, proteincinasas (p. ej., la proteincinasa activada por mitógeno o MAPK) y factores de transcripción, que van a producir mediadores proinflamatorios e inducen la activación de células dendríticas, que a su vez van a facilitar la activación del sistema inmunitario11. En cualquier caso, inmunidad innata y adaptativa se activan de forma conjunta12, esta circunstancia podría condicionar una mayor facilidad de los pacientes con ECI o dermatitis atópica para sensibilizarse ante antígenos débiles, como las fragancias13.
El evento inicial que va a provocar la reacción inflamatoria va a ser el daño a la barrera cutánea y el daño celular14. Los queratinocitos desempeñan un papel clave en la respuesta inflamatoria al liberar citocinas, sobreexpresar los antígenos del complejo mayor de histocompatibilidad (CMH) tipo II y expresando moléculas de adhesión celular. La interacción entre la barrera cutánea y la respuesta inmunitaria es bidireccional, de forma que diversas citocinas pueden provocar un deterioro de la barrera cutánea al alterar la producción de proteínas importantes en la formación del estrato córneo como la loricrina y la profilagrina.
La principal citocina responsable de iniciar la cascada inflamatoria es la IL-1α11. Existe un depósito preformado de está citocina en la capa córnea y en los queratinocitos, que se libera al degradarse la capa córnea tras el contacto con los irritantes. El factor de necrosis tumoral α (TNF-α) sería otra de las citocinas que desempeña un papel fundamental en perpetuar la respuesta inflamatoria, al aumentar la expresión del CMH tipo II y las moléculas de adhesión celular (ICAM) I. Se ha visto que polimorfismos en los genes que se encargan de la expresión del TNF-α pueden suponer un factor de riesgo para el ECI15. Por otro lado, se ha visto que hay citocinas que pueden tener un papel protector frente al ECI, como la interleucina (IL) 6 y el receptor α de la IL-6 (IL-6Rα) 16,17, implicados de forma clave en la regeneración de la piel. Se ha comprobado in vitro que la pérdida de expresión de estas moléculas aumenta la respuesta inflamatoria ante irritantes.
En la dermis, la liberación de citocinas va a inducir el reclutamiento de células inflamatorias como linfocitos, mastocitos, neutrófilos o histiocitos al tiempo que se produce una cronificación de la inflamación11. Existe evidencia de que hay células que tendrían un papel protector, como las células mieloides inmaduras Gr1+CD11b+ 18. Estás células representan un grupo heterogéneo de células (macrófagos, granulocitos y células dendríticas) en estadios tempranos de maduración, que tienen potencialmente capacidad para disminuir la producción de citocinas y de células T. La expresión de estas células está condicionada por la vía del fosfatidilinositol 4,5 bifosfato. Se ha comprobado que cuando una de las enzimas que la regula, la fosfolipasa Cδ1, no se expresa, la respuesta inflamatoria ante irritantes está disminuida y la expresión de las células mieloides inmaduras Gr1+CD11b+ se encuentra aumentada.
Contenido relacionado
Factores predisponentes al eczema de contacto irritativo
El ECI va a estar condicionado por una serie de factores que dependen del paciente, del ambiente donde va a tener lugar la agresión y de las características del irritante.
El paciente
Edad
La edad de los pacientes no se ha podido correlacionar de forma adecuada con una mayor predisposición al ECI. La mayoría de los pacientes tienen una edad media6 que coincide con la etapa más activa laboralmente, ya que la causa más frecuente es la exposición profesional. Los pacientes ancianos tienen una piel seca debido al menor contenido de lípidos de su piel, su piel no cura de forma rápida, por lo que la barrera cutánea está alterada1 y van a desarrollar más fácilmente eczema asteatósico y ECI perineal. Por otro lado, en los niños es frecuente encontrar dermatitis del pañal, dermatitis plantar juvenil o dermatitis perioral, que también tienen un componente irritativo.
Sexo
El ECI es más frecuente en las mujeres, sin embargo cuando se han hecho pruebas de exposición con lauril sulfato sódico, cloruro de benzalconio, cantaridina o aceite de crotón no se han encontrado diferencias por sexo8, por lo que parece que la mayor frecuencia de ECI estaría asociada posiblemente al hecho de que además de contactar con irritantes en el trabajo, tienen una mayor exposición a los irritantes en el hogar.
Localización
El ECI tiene más facilidad para producirse en localizaciones con la piel más fina, P. Mercader 44 Eczema-dermatitis. Manual diagnóstico y terapéutico como la cara, los espacios interdigitales y el dorso de las manos, por el menor espesor de la capa córnea; también se afectan más las zonas con pliegues, como los párpados o la zona interdigital por la mayor retención de los irritantes.
Atopia
Los pacientes atópicos tienen un mayor riesgo de desarrollar un eczema de manos cuando se exponen a irritantes7 . Las mutaciones del gen de la filagrina que se encuentra en los pacientes atópicos producen una alteración de la barrera cutánea que produce una menor tolerancia a los irritantes y una mayor permeabilidad a los antígenos19.
Otros factores
La susceptibilidad individual a padecer ECI es muy variable y posiblemente influyan otros factores genéticos independientes de la atopia, como los polimorfismos del TNF-α15, mutaciones de filagrina no asociadas a dermatitis atópica20 o en el gen de la IL-1α21.
Ambiente
Factores ambientales como la humedad, la temperatura, el flujo de aire o la oclusión afectan la respuesta de la piel ante los irritantes. La temperatura fría y la baja humedad aumentan la pérdida transepidérmica de agua22, facilitando la aparición de grietas y descamación. Por otro lado una humedad excesiva también puede alterar la barrera cutánea23, degradando el estrato córneo y aumentando la permeabilidad ante antígenos e irritantes. La fricción crónica y los microtraumas repetidos también va a provocar una alteración del estrato córneo, haciendo que la piel sea más susceptible a los irritantes y alérgenos.
Existen varias profesiones que reúnen una o varias de estas condiciones, y que además tienen una mayor frecuencia de contacto con irritantes como jabones, detergentes, agua, cáusticos y otras sustancias químicas u orgánicas. Algunas de las profesiones con una mayor frecuencia de ECI son: personal sanitario, peluqueras, metalúrgicos, manipuladores de alimentos y trabajadores de la construcción.
Irritantes
Los irritantes son sustancias físicas o químicas con capacidad para producir daño celular cuando entran en contacto con la piel durante el tiempo suficiente o a concentraciones elevadas. Los irritantes más frecuentes son el agua/trabajo húmedo, diferentes tipos de productos químicos y los irritantes físicos.
Agua y trabajo húmedo
El contacto continuado con el agua es posiblemente el factor irritante más frecuente. Este contacto es más frecuente en el medio laboral, y por eso se habla de «trabajo húmedo», donde se engloba no solo el contacto directo con el agua, sino también otros factores como, por ejemplo, la humedad producida por la sudoración de las manos y el uso de guantes. Los criterios para definir el trabajo húmedo incluyen7:
-
Tener las manos más de dos horas al día en un ambiente húmedo.
-
Lavado frecuente de manos (> 20 veces al día).
-
Usar más de 20 veces desinfectantes de manos en una jornada laboral.
-
Usar guantes de protección más de dos horas al día o cambiar de guantes más de 20 veces al día. Aunque se cumplan estas condiciones, hay una gran variabilidad individual en el desarrollo de ECI, y no todos los pacientes sometidos a trabajo húmedo van a acabar desarrollando un eczema de manos. Ni el hacer trabajo húmedo excluye estudiar al paciente para descartar otros tipos de eczema.
Irritantes químicos
Dependiendo del tipo de producto químico, la respuesta inflamatoria va a seguir diferentes vías22. Según la reacción que producen, estos se clasifican en:
-
Irritantes agudos, como los ácidos y las bases fuertes, que van a producir un daño agudo y rápido en la piel, produciendo quemaduras y úlceras (Fig. 1).
-
Irritantes agudos retardados, como el cloruro de benzalconio, presente en antisépticos, productos cosméticos y productos oftalmológicos, que producen una respuesta rápida, pero no inmediata.
-
Irritantes acumulativos, como el agua o los surfactantes de los jabones, que precisan una exposición repetida para producir lesiones.
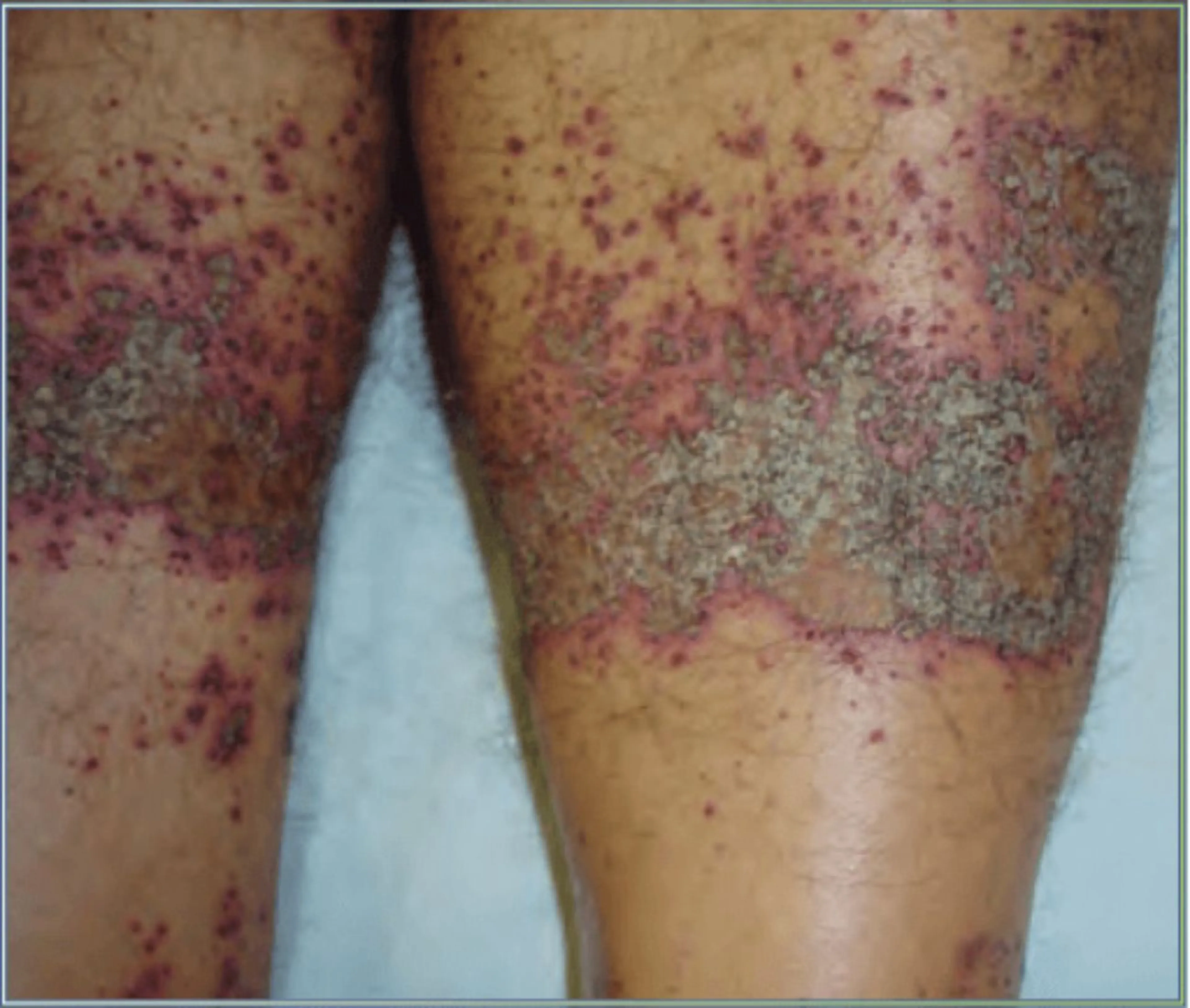
Figura 1. Quemadura producida por cemento fresco. El cemento fresco es una base con un pH muy elevado y es frecuente que los albañiles novatos tengan eczemas de contacto irritativo agudos que simulan quemaduras cuando entran en contacto con él.
Irritantes físicos
El polvo es una causa frecuente de dermatitis irritativa aerotransportada; se entiende por polvo una sustancia sólida lo suficientemente ligera como para mantenerse en el aire, como por ejemplo el serrín o el cemento en polvo. Van a producir una dermatitis seca y liquenificada, frecuentemente con un patrón folicular1 . Otro irritante físico muy frecuente es la lana, que es una causa relativamente frecuente de dermatitis en niños.
Clínica
De forma genérica, las dermatitis irritativas se caracterizan por ser lesiones bien delimitadas, limitadas a la zona de aplicación del agente responsable (Fig. 2) y con poco prurito. Muchos pacientes hablan de dolor o de sensación de quemazón. La morfología clínica del ECI es muy variada y puede ir desde un discreto eritema y descamación a unas lesiones más extensas con vesiculación, indistinguible del ECA. En un intento de armonizar las definiciones, en 1997 se publicó un documento de consenso24 que incluía nueve tipos de ECI. Posteriormente, Chew y Maibach25 los aumentaron a 10. Esta clasificación aparece resumida en la tabla 1 y, aunque parece adecuada desde un punto de vista académico, resulta algo confusa porque algunas entidades se solapan (p. ej., el ECI crónico con la reacción irritante). Otras clasificaciones se han basado en la morfología clínica, la localización anatómica, los grupos de personas afectadas, la vía de contacto o la naturaleza del agente irritante. Para una mejor comprensión de la clínica he considerado preferible explicar las entidades clínicas específicas más frecuentes.
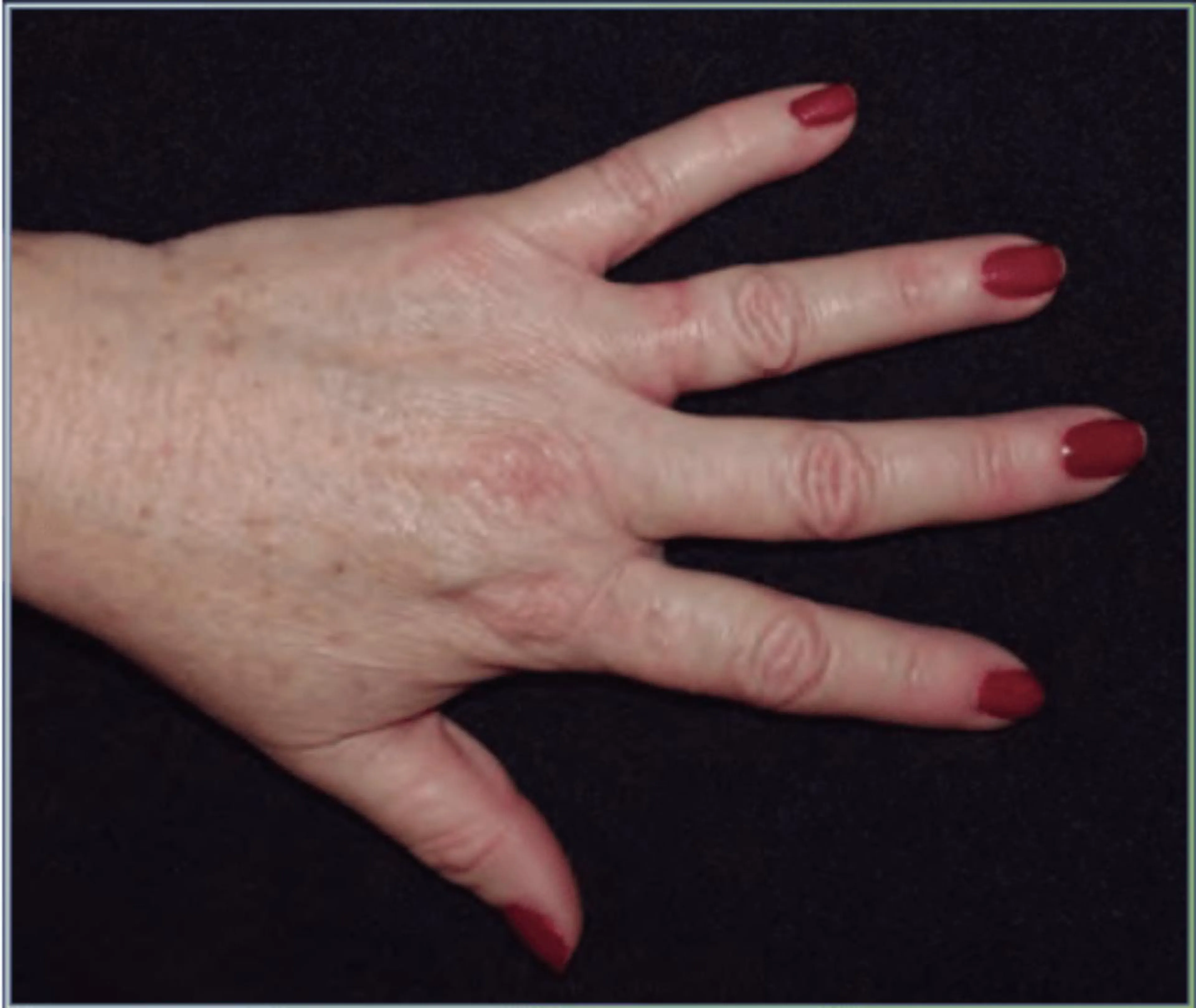
Figura 2. Eczema de contacto irritativo localizado en el dedo. Es muy típica la aparición de eczemas debajo dee los anillos por la acumulación de las sustancias irritantes en la zona.
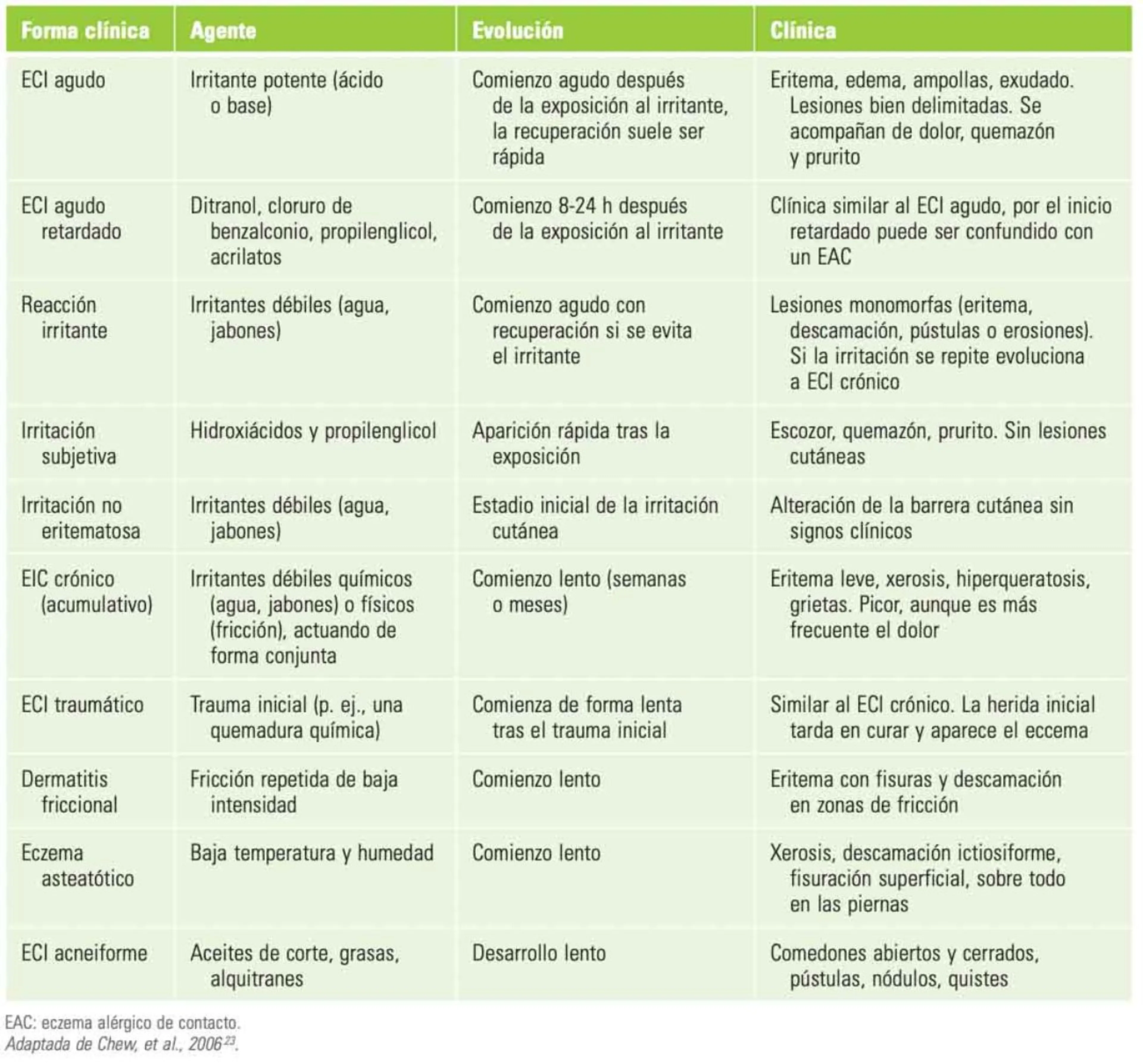
Tabla 1. Formas clínicas de eczema de contacto irritativo (ECI)
Eczema de contacto irritativo crónico
También conocido como ECI acumulativo, porque necesita que la irritación se produzca de forma repetida, con poco intervalo entre las aplicaciones del irritante, que impiden que se recupere la barrera cutánea de forma completa. El daño se va acumulando hasta que supera un determinado umbral. A partir de que ese umbral se supera, agresiones leves, aunque estén más separadas en el tiempo, pueden producir lesiones clínicas apreciables. El ECI crónico es más frecuente con irritantes leves que actúan de forma conjunta, tanto químicos como físicos, incluyendo microtraumas, fricción, la baja humedad, la temperatura o el efecto desecante del polvo11. Los pacientes atópicos tienen una tolerancia disminuida a los irritantes y un tiempo de recuperación de la barrera cutánea aumentado, por lo que son más susceptibles de desarrollar un ECI crónico. La localización más frecuente del ECI crónico son las manos y antebrazos, con aparición de eritema, descamación y fisuras, sin vesículas. Suelen comenzar en los pliegues interdigitales y se van extendiendo por el dorso y la cara palmar de los dedos. Es típica la acentuación de los pliegues palmares (hiperlinealidad palmar) (Fig. 3), mientras que en los pulpejos se produce una pérdida de los dermatoglifos26. Clásicamente, este tipo de dermatitis se veía más en mujeres en relación con las tareas propias del hogar, por lo que recibió el nombre de «dermatitis del ama de casa». Sin embargo, es una denominación que puede inducir a error, ya que no es específico de las mujeres, y también se puede dar en otros trabajos que conlleven la exposición a detergentes, limpiadores y al trabajo húmedo, como los camareros o el personal de limpieza, por lo que es preferible evitar ese término.
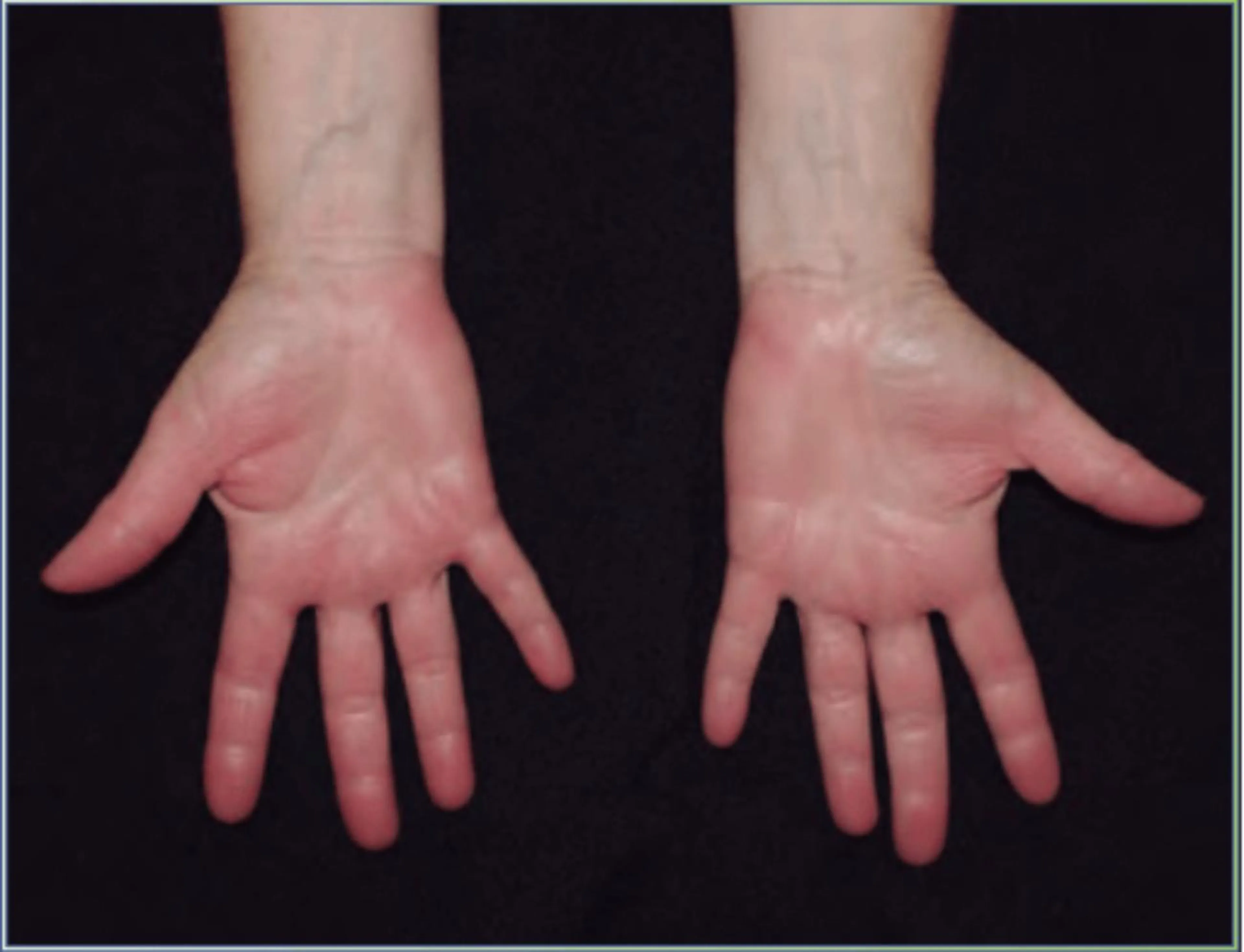
Figura 3. Eczema de contacto irritativo crónico en una camarera, se aprecia la hiperlinealidad palmar y la perdida de dermatoglifos con un eritema leve.
Eczema de contacto irritativo del área del pañal, dermatitis del pañal
El término de dermatitis del pañal es un término usado por los clínicos para referirse a cualquier erupción en la zona del pañal, aunque puede tener una etiología muy variada; lo más frecuente es que se trate una dermatitis irritativa provocada por el contacto mantenido con la orina y las heces. Clínicamente es típica la afectación de las nalgas, periné y los genitales, respetando los pliegues inguinales con un patrón que se conoce como patrón en W. En casos extremos se pueden ver lesiones ulceradas (Fig. 4) (sifílides papuloerosivas de Jaquet Silvestri) o nodulares (granuloma glúteo infantil). La prevalencia de dermatitis del pañal en niños ha disminuido desde que se usan pañales desechables, sin embargo, el aumento de la esperanza de vida ha aumentado el uso de pañales en la población anciana, por los problemas de incontinencia asociados a la senectud, por lo que es un problema relativamente frecuente en esta población27.
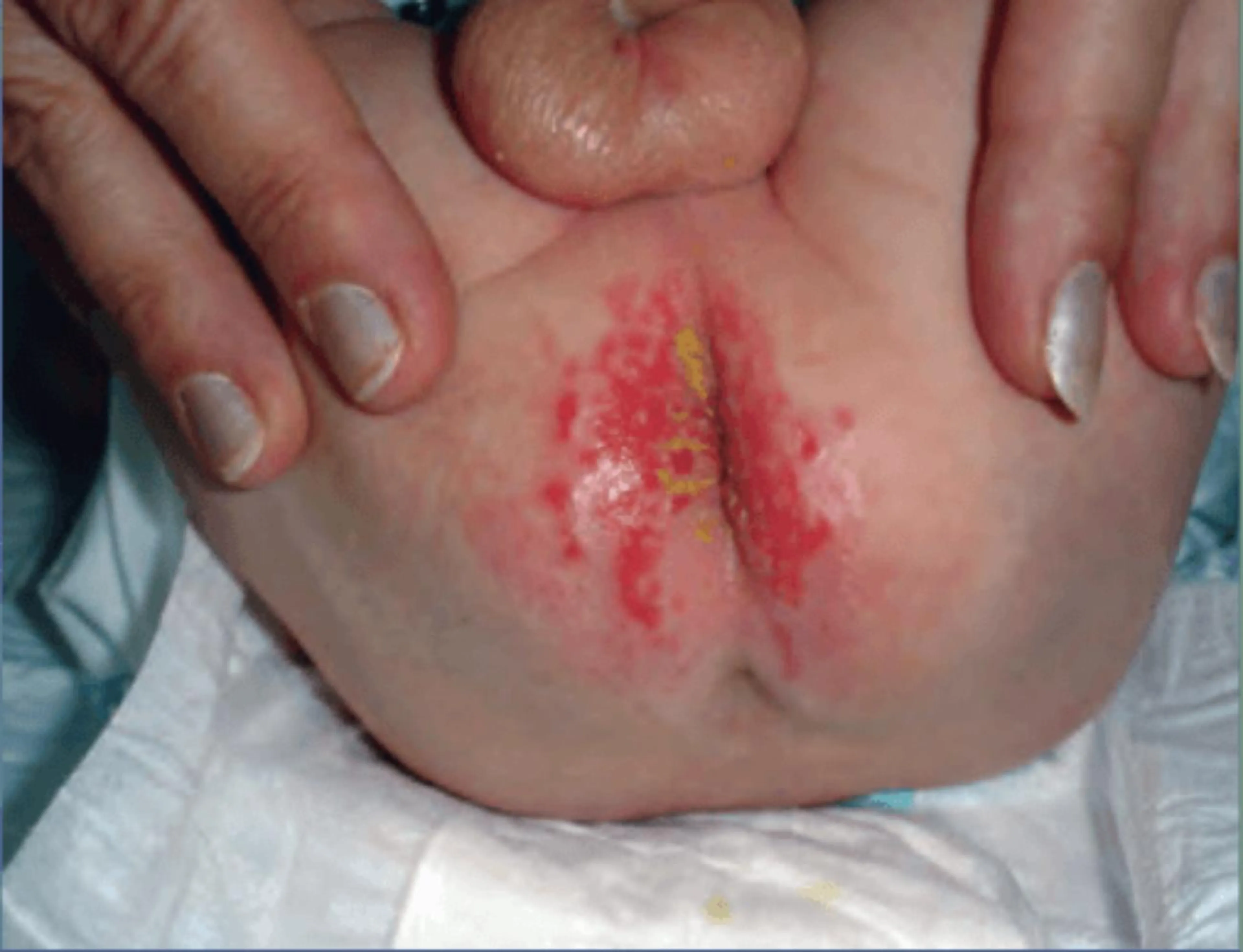
Figura 4. Lesiones ulceradas en la zona del pañal. Es frecuente que estas lesiones aparezcan cuando los niños presentan diarrea y las heces son más líquidas y abundantes.
Eczema de contacto irritativo hiperqueratósico palmar
Esta forma de eczema irritativo es típica de varones adultos en cuyo trabajo hay contacto con aceites minerales, grasas o disolventes, y que además realizan fuerza o presión con las manos. Es muy típico en mecánicos, agricultores o metalúrgicos. Clínicamente se caracteriza por lesiones hiperqueratósicas y fisuradas con afectación de la cara palmar de las manos. Además, suele haber una hiperpigmentación, más acentuada en las grietas, de origen exógeno por el contacto con las sustancias químicas que lo provocan (Fig. 5). El eczema hiperqueratósico palmar irritativo debe diferenciarse del eczema hiperqueratósico palmar endógeno7 , donde no hay un contacto conocido con irritantes. Está entidad se solapa y es difícil de diferenciar de otras enfermedades con afectación palmar como la neurodermitis y, sobre todo, la psoriasis palmar.
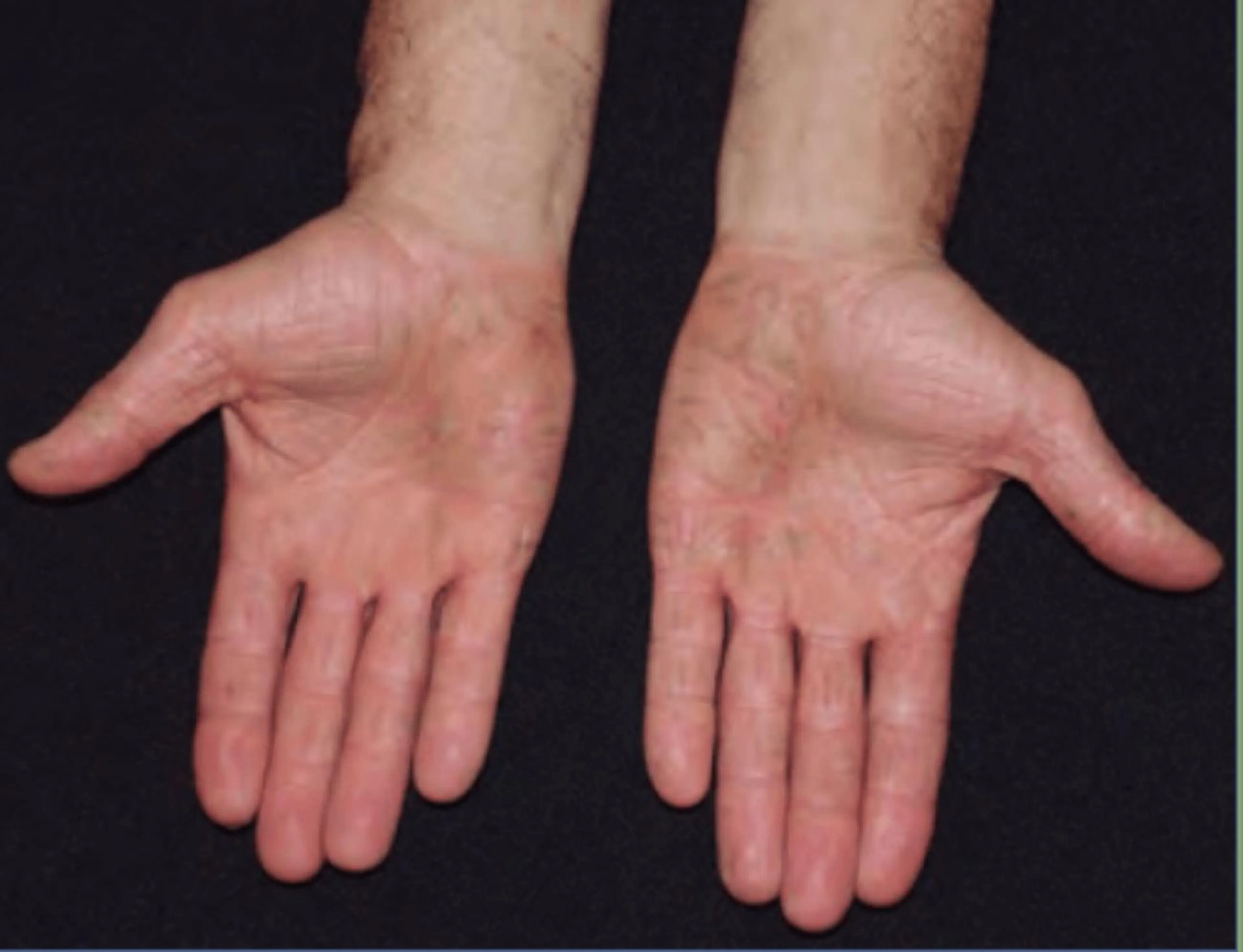
Figura 5. Eczema hiperqueratósico palmar en un fontanero.
Eczema de contacto irritativo de los pulpejos de los dedos o pulpitis irritativa
Se trata de una forma de ECI que se limita a los pulpejos de los dedos. Se produce en trabajos con fricción constante, como por ejemplo los cortadores de mármol. Clínicamente se presenta con descamación y fisuración de los pulpejos y es muy difícil de diferenciar de la pulpitis alérgica de contacto producida por el ajo o la alstromeria.
Eczema de contacto irritativo de localización perioral
Es típica de niños que tienen el hábito de succionarse los labios, por la maceración provocada por el contacto con la saliva. Clínicamente se observa un eritema con descamación localizado en la zona donde el niño se toca con la lengua, de manera que las lesiones están muy bien delimitadas. Está forma de dermatitis debe diferenciarse de una forma de rosácea que también se ve en niños y que presenta unas pápulas monomorfas sobre una base eritematosa, que recibe el mismo nombre. Es importante distinguir ambos cuadros clínicos, porque la dermatitis irritativa se puede tratar con corticosteroides. Por el contrario, la rosácea puede empeorar con ese tratamiento.
Eczema de contacto irritativo en áreas de xerosis cutánea o eczema asteatósico (ezcématide por desecación/eczema craquelé)
El eczema asteatósico predomina en las piernas de personas mayores en los meses de invierno. Esta enfermedad se produce sobre todo por la baja humedad y el frío de los meses de invierno, aunque otros factores (trabajo húmedo, fricción, contacto con químicos) pueden contribuir al desarrollo de las lesiones. Clínicamente se aprecia xerosis, una descamación ictiosiforme y grietas superficiales, sobre una base eritematosa. Probablemente, la dermatitis invernal del dorso de las manos26 represente una forma de eczema asteatósico, ya que la morfología de las lesiones es muy similar y además se producen también en los meses de invierno.
Eczema de contacto irritativo de las plantas de los pies o dermatitis plantar juvenil
Las lesiones se producen sobre todo en pacientes atópicos. Se aprecia eritema y descamación en el tercio anterior de ambos pies, siendo característica la afectación de los pulpejos de los primeros dedos. La hiperhidrosis y el llevar calzado oclusivo, sobre todo de plástico, se relaciona con la aparición de las lesiones y los brotes de empeoramiento, siendo una de las razones por las que estas lesiones parece que se dan más en verano28.
Dermatitis pustular y acneiforme de origen irritativo
dos de corte y productos clorados puede producir una dermatitis pustular y acneiforme, sobre todo en pacientes atópicos11. No todos los individuos expuestos a estos productos van a desarrollar lesiones, por lo que la susceptibilidad individual es un factor determinante. El acné profesional que se produce tras el contacto con productos derivados del petróleo se conoce también como botón de aceite, y es típico de mecánicos y operadores de fábricas. Las lesiones son comedones abiertos, cerrados, nódulos y pústulas, que predominan en las manos y los antebrazos. Los aceites pueden impregnar las ropas de trabajo y producir lesiones también en las zonas cubiertas. Otro factor etiológico en estos casos es la irritación mecánica producida por la fricción y el roce. El cloracné se produce por la exposición ambiental o laboral a compuestos clorados orgánicos, como las dioxinas. En estos casos, los pacientes suelen tener una coloración amarillenta de la piel además de las lesiones acneiformes.
Eczema de contacto irritativo aerotransportado
El ECI aerotransportado está causado por sustancias presentes en el aire que se depositan en la piel. La mayoría de los irritantes aerotransportados se encuentran en el ambiente laboral y pueden ser partículas de polvo, gases, espráis, vapores o fibras. Las lesiones tienden a localizarse en zonas expuestas como la cara, el cuello, el escote o el dorso de las manos. En la cara, los párpados superiores son especialmente susceptibles al ser una piel muy fina. Algunas veces las lesiones pueden afectar zonas cubiertas, especialmente los pliegues, porque las sustancias quedan atrapadas en la ropa y tienden a localizarse en esa zona. Las lesiones clínicas y la severidad van a depender del tipo de irritante y del grado de exposición. Podemos encontrar pequeñas pápulas, lesiones lineales escoriadas por el rascado o una erupción maculopapular. Si hay exposición a vapores o gases irritantes podemos encontrar lesiones agudas.
Diagnóstico
El diagnóstico del ECI se basa en la historia clínica, la exploración física y en la realización de pruebas epicutáneas que descarten la existencia de algún alérgeno relevante. Es un proceso intuitivo que depende en gran medida de la experiencia del médico que está examinando al paciente para detectar la existencia de una exposición al irritante y asociarlo de una manera fiable a la clínica del paciente.
Historia clínica
La historia clínica debe permitir evaluar todos los posibles desencadenantes. En el ámbito laboral se debe hacer una descripción del tipo de trabajo que hace el paciente, incluyendo las sustancias que manipula, el ambiente en el que se desarrolla el trabajo, las condiciones de humedad, temperatura o exposición a la radiación UV, qué medidas de protección se siguen y las medidas de limpieza que se toman. Si se sospecha que el origen es laboral, muchas veces es preciso realizar una visita al lugar de trabajo para evaluar todas esas variables. También se deben comprobar las exposiciones no laborales, conocer qué aficiones tiene el paciente, qué productos manipula en el hogar y los tratamientos que ha realizado previamente. La valoración de la exposición debe incluir datos cuantitativos, como la frecuencia y duración de la exposición, y la extensión de piel expuesta. También se deben valorar otros factores concomitantes como la presencia de fricción, oclusión o traumatismos. Algunas veces no se puede identificar de una manera apropiada las fuentes de exposición porque los pacientes no son capaces de detectarlas cuando la exposición es esporádica o infrecuente. En otras ocasiones, la fuente del contacto es desconocida porque los fabricantes no identifican de forma adecuada los productos químicos en las fichas de datos de seguridad o en las etiquetas de los productos. Una vez que se han valorado los posibles desencadenantes, es esencial conocer la relación temporal entre la exposición y la aparición de las lesiones. La aparición de lesiones de forma rápida tras la primera exposición iría a favor de que se trata de un ECI. No obstante, el ECI crónico requiere exposiciones repetidas y es más difícil de diferenciar de un ECA. En cuanto a los síntomas subjetivos, el ECI se acompaña de sensación de quemazón y dolor, mientras que en el ECA el síntoma que predomina es el picor.
Exploración física
Las características de las lesiones clínicas y su distribución pueden dar pistas sobre el causante del eczema y para distinguir un ECA de un ECI. No obstante, ninguna de esas características es patognomónica. De este modo, la presencia de vesículas en las caras laterales de los dedos y en la palma de la mano son típicos del eczema dishidrótico. Pero algunas sustancias pueden inducir un EAC o un ECI de características similares. Un problema adicional en la valoración del eczema de manos es que, de forma frecuente, son multifactoriales, de manera que coexisten factores alérgicos, irritantes y endógenos. Los datos que nos ayudan a identificar un ECI son: – De forma general las lesiones están localizadas en la zona de contacto con el irritante, mientras que en el EAC las lesiones se suelen extender más allá de la zona de contacto. – El ECI agudo puede cursar con úlceras y zonas de necrosis, que en el EAC no suelen aparecer. – La localización del dorso de las manos, de los dedos y, sobre todo, de los espacios interdigitales es muy característica del ECI crónico secundario a trabajo húmedo.
Anatomía patológica
Las biopsias tienen un papel limitado para diferenciar entre un ECI o un EAC29. Si la biopsia se obtiene en los momentos iniciales de la irritación se pueden observar algunos signos que podrían ser útiles para hacer el diagnóstico diferencial. Sobre todo, porque los mecanismos de producción de las lesiones son diferentes: en el ECI predomina el daño a la epidermis, mientras que en el EAC se produce una respuesta inflamatoria por los linfocitos de la dermis. En el caso de biopsias de ECI se observa necrosis de queratinocitos e infiltrados de neutrófilos en la dermis, con pocos linfocitos y eosinófilos. Estos signos suelen desaparecer cuando las lesiones se cronifican. En las lesiones crónicas, la presencia de eosinófilos iría a favor de EAC, mientras que la ausencia de exocitosis de linfocitos iría a favor de ECI. Sin embargo, son datos muy sutiles, y en la práctica clínica son difícilmente valorables.
Pruebas epicutáneas y prick test
Aunque clínicamente las lesiones sugieran un ECI, en todos los casos de eczemas persistentes que no responden al tratamiento es indispensable realizar pruebas epicutáneas para descartar un EAC. Si los pacientes usan guantes de látex y se sospecha una urticaria de contacto, también sería recomendable realizar un prick test. Está prueba también sería recomendable en el caso de sospechar una dermatitis de contacto por proteínas.
Contenido relacionado
Manejo de los pacientes
Los principios del manejo del ECI incluyen la evitación, protección y sustitución del irritante. Las medidas preventivas son fundamentales y deben hacerse en todos los casos, tanto como medida de prevención primaria como en el tratamiento de los casos que ya han desarrollado el ECI. Los agentes causales deben ser evitados y la exposición a otros posibles irritantes como jabones o detergentes debe ser limitada. Es importante recordar que cualquier material puede acabar actuando como un irritante de la piel si la piel se expone a concentraciones elevadas durante el tiempo suficiente.
Prevención
Las principales medidas de prevención primaria deben llevarse a cabo en la organización de las empresas, impulsando la automatización del trabajo y sustituyendo las sustancias irritantes por otras menos agresivas. Una vez que estas medidas se han llevado a cabo, debe instruirse al trabajador en medidas de protección individuales como el uso de guantes, cremas barrera o medidas de limpieza30. La evidencia para el uso de algunas de estas intervenciones se ha publicado en una reciente revisión sistemática31 y serían útiles tanto para la prevención primaria como para la secundaria.
Programas de educación para cuidar la piel
Los programas de educación para cuidado de la piel que se han hecho entre los trabajadores para prevenir el desarrollo de ECI parecen tener una utilidad limitada. En una revisión sistemática31, un 21% de los pacientes que habían implementado los programas educativos tenían lesiones, frente a un 28% en el grupo control.
Cremas barrera y cremas emolientes
Algunos autores31 diferencian entre crema barrera y cremas emolientes, por las características de las cremas y el momento de aplicación. Es controvertido si existe esa distinción, porque muchas cremas barrera y cremas emolientes comparten componentes parecidos. Las cremas barrera son preparados que intentan crear una capa fina en la piel que la proteja de la irritación. Esa capa está pensada para facilitar la eliminación de los contaminantes y limitar el daño producido por el lavado frecuente de manos. Además, las cremas barrera pueden tener ingredientes activos que transformen o atrapen los irritantes. Se recomienda su uso antes del trabajo y después 2-3 veces durante la jornada laboral, según sea necesario. Las cremas emolientes son cremas que se usan para regenerar la piel. Tienen una amplia variedad de componentes diseñados para incrementar la hidratación de las capas externas de la piel, al reducir la pérdida de agua de la piel. Han demostrado que previenen la irritación cutánea producida por detergentes y que aceleran la reparación de la piel irritada31. Deben usarse de forma regular durante el trabajo, después de cada lavado de manos y también en casa, cuando se realizan trabajos propios del hogar.
Guantes
Los guantes de protección son indispensables para la prevención del ECI. Deben ser adecuados al tipo de trabajo que se realice. Sin embargo, el uso no adecuado de los guantes puede ser un factor que contribuya al empeoramiento del eczema11 por la maceración provocada por el sudor y la fricción provocada por los guantes. Además, de manera accidental pueden quedar sustancias dentro del guante que, por efecto de la oclusión, pueden multiplicar el daño que provocan. Es importante asegurarse de que los guantes no tienen punciones o grietas que permitan el paso de los irritantes y cambiar los guantes de manera regular para reducir la transpiración y el sudor. Por este mismo motivo, también es recomendable el uso de un guante de algodón debajo del guante de goma. El uso de guantes junto con cremas barrera y emolientes son las medidas recomendables31 para evitar la aparición de un ECI en aquellas profesiones con riesgo para la piel.
Tratamiento
El uso de corticosteroides tópicos tiene un papel limitado en el tratamiento del ECI. Evitar la exposición al irritante es la medida más eficaz, y los corticosteroides pueden ser útiles en la disminución de la inflamación, aunque para algunos autores pueden alterar la barrera cutánea. El uso de tacrolimús tópico en la inflamación y en la síntesis de ceramidas de la piel irritada tiene un efecto similar al de corticosteroides como la betametasona32. También se ha confirmado el efecto antiinflamatorio del pimecrolimús en la cara y el cuello33. Otro tratamiento que se ha usado es el psoraleno y radiación ultravioleta A (PUVA) en pacientes refractarios a otros tratamientos.
Conclusiones
- El ECI es probablemente la enfermedad profesional más frecuente.
- El ECI va a estar condicionado por una serie de factores que dependen del paciente, del ambiente donde ocurre la agresión y de las características del irritante.
- Existen diferentes formas clínicas de ECI, que en muchos casos coexiste con el eczema atópico o el EAC.
- El diagnóstico del ECI se basa en la historia clínica, la exploración física y en la realización de pruebas epicutáneas que descarten la existencia de algún alérgeno relevante.
- Los principios del manejo del ECI incluyen la evitación, la protección y la sustitución del irritante causante de las lesiones, medidas que pueden ser más eficaces que el tratamiento farmacológico.

Dr. P. Mercader García
Médico especialista en dermatología, Hospital Morales Meseguer, Murcia.
Temas relacionados:
#Dermatología #Alergología #Inflamación tipo 2
Actualidad Científica

Referencias
- Bains SN, Nash P, Fonacier L. Irritant contact dermatitis. Clin Rev Allergy Immunol. 2019;56(1):99-109.
- Mathias CG. Contact dermatitis and workers’ compensation: Criteria for establishing occupational causation and aggravation. J Am Acad Dermatol. 1989;20(5):842-8.
- Holness DL. Characteristic features of occupational dermatitis: epidemiologic studies of occupational skin disease reported by contact dermatitis clinics. Occup Med. 1994;9(1):45-52.
- Higgins CL, Palmer AM, Cahill JL, Nixon RL. Occupational skin disease among Australian healthcare workers: a retrospective analysis from an occupational dermatology clinic, 1993-2014. Contact Dermatitis. 2016; 75(4):213-22.
- Rietschel RL, Mathias CGT, Fowler JF, Pratt M, Taylor JS, Sherertz EF, et al. Relationship of occupation to contact dermatitis: Evaluation in patients tested from 1998 to 2000. Am J Contact Dermat. 2002;13(4):170-6.
- Pesonen M, Jolanki R, Larese Filon F, Wilkinson M, Kre˛cisz B, Kiec’-S’wierczyn’ska M, et al. Patch test results of the European baseline series among patients with occupational contact dermatitis across Europeanalyses of the European Surveillance System on Contact Allergy network, 2002-2010. Contact Dermatitis. 2015;72(3):154-63.
- Agner T, Aalto-Korte K, Andersen KE, Foti C, GimenézArnau A, Goncalo M, et al. Classification of hand eczema. J Eur Acad Dermatology Venereol. 2015; 29(12):2417-22.
- Belsito DV. Occupational contact dermatitis: Etiology, prevalence, and resultant impairment/disability. J Am Acad Dermatol. 2005;53(2):303-13.
- Diepgen TL, Coenraads PJ. The epidemiology of occupational contact dermatitis. Int Arch Occup Environ Health. 1999;72(8):496-506.
- Matzinger P. The danger model: A renewed sense of self. Science. 2002;296:301-5.
- Ale IS, Maibach HI. Irritant contact dermatitis. Rev Environ Health. 2014;29(3):195-206.
- Martin SF. The role of the innate immune system in allergic contact dermatitis. Allergol Sel. 2017;1(1):39-43.
- Kohli N, Nedorost S. Inflamed skin predisposes to sensitization to less potent allergens. J Am Acad Dermatol. 2016;75(2):312-7.e1.
- Jakasa I, Thyssen JP, Kezic S. The role of skin barrier in occupational contact dermatitis. Exp Dermatol. 2018; 27(8):909-14.
- De Jongh CM, John SM, Bruynzeel DP, Calkoen F, van Dijk FJH, Khrenova L, et al. Cytokine gene polymorphisms and susceptibility to chronic irritant contact dermatitis. Contact Dermatitis. 2008;58(5):269-77.
- Frempah B, Luckett-Chastain LR, Calhoun KN, Gallucci RM. Keratinocyte-specific deletion of the IL-6RΑ exacerbates the inflammatory response during irritant contact dermatitis. Toxicology. 2019;423(May 2019):123-31.
- Frempah B, Luckett-Chastain LR, Gallucci RM. IL6Rα function in myeloid cells modulates the inflammatory response during irritant contact dermatitis. Exp Dermatol. 2019;28(8):948-55.
- Shiratori K, Kanemaru K, Ogura T, Nakajima A, Sugizaki Y, Fukuyama T, et al. Epidermal loss of phospholipase Cδ1 attenuates irritant contact dermatitis. Biochem Biophys Res Commun. 2019;511(2):330-5.
- Scharschmidt TC, Man MQ, Hatano Y, Crumrine D, Gunathilake R, Sundberg JP, et al. Filaggrin deficiency confers a paracellular barrier abnormality that reduces inflammatory thresholds to irritants and haptens. J Allergy Clin Immunol. 2009;124(3).
- Timmerman JG, Heederik D, Spee T, van Rooy FG, Krop EJM, Koppelman GH, et al. Contact dermatitis in the construction industry: The role of filaggrin loss-offunction mutations. Br J Dermatol. 2016;174(2):348-55.
- Landeck L, Visser M, Kezic S, John SM. IL1A-889 C/T gene polymorphism in irritant contact dermatitis. J Eur Acad Dermatology Venereol. 2013;27(8):1040-3.
- Uter W, Gefeller O, Schwanitz HJ. An epidemiological study of the influence of season (cold and dry air) on the occurrence of irritant skin changes of the hands. Br J Dermatol. 1998;138(2):266-72.
- Ogawa-Fuse C, Morisaki N, Shima K, Hotta M, Sugata K, Ichihashi T, et al. Impact of water exposure on skin barrier permeability and ultrastructure. Contact Dermatitis. 2019;80(4):228-33.
- Moshell AN. Workshop on irritant contact dermatitis. Am J Contact Dermat. 1997;8(2):79-105.
- Chew AL, Maibach HI. Ten genotypes of irritant contact dermatitis. En: Chew AL, Maibach HI, editores. Irritant Dermatitis. Berlin: Springer-Verlag; 2006. pp. 5-9.
- de la Cuadra-Oyanguren J. Dermatitis de contacto irritativa. Piel. 1988;3(9):413-23.
- Foureur N, Vanzo B, Meaume S, Senet P. Prospective aetiological study of diaper dermatitis in the elderly. Br J Dermatol. 2006;155(5):941-6.
- Silverberg NB. Typical and atypical clinical appearance of atopic dermatitis. Clin Dermatol. 2017;35(4):354-9.
- Frings VG, Böer-Auer A, Breuer K. Histomorphology and immunophenotype of eczematous skin lesions revisited-skin biopsies are not reliable in differentiating allergic contact dermatitis, irritant contact dermatitis, and atopic dermatitis. Am J Dermatopathol. 2018;40(1):7-16.
- Alfonso JH, Bauer A, Bensefa-Colas L, Boman A, Bubas M, Constandt L, et al. Minimum standards on prevention, diagnosis and treatment of occupational and workrelated skin diseases in Europe - position paper of the COST Action StanDerm (TD 1206). J Eur Acad Dermatology Venereol. 2017;31:31-43.
- Bauer A, Rönsch H, Elsner P, Dittmar D, Bennett C, Schuttelaar MLA, et al. Interventions for preventing occupational irritant hand dermatitis. Cochrane Database Syst Rev. 2018;4(4):CD004414.
- Jungersted JM, Høgh JK, Hellgren LI, Jemec GBE, Agner T. Effects of topical corticosteroid and tacrolimus on ceramides and irritancy to sodium lauryl sulphate in healthy skin. Acta Derm Venereol. 2011;91(3):290-4.
- Mensing CO, Mensing CH, Mensing H. Treatment with pimecrolimus cream 1% clears irritant dermatitis of the periocular region, face and neck. Int J Dermatol. 2008;47(9):960-4

Realice el Test de Control de dermatitis atópica (ADCT)
La dermatitis atópica, un tipo de eccema, puede estar afectando la vida de su paciente en más formas de las que cree.
El ADCT da una medida de qué tan controlado está el eczema. Responda estas 6 preguntas simples con su paciente para encontrar la puntuación ADCT. Indicará el curso de acción adecuado.
Encuentre la puntuación de su pacienteMAT-ES-2102158 V1 Junio 2021